Por detrás das clínicas e das brocas, equipas de laboratório procuram uma solução mais fiel.
Dados recentes em ratos sugerem um caminho vivo para a regeneração de raízes danificadas e suporte da mandíbula. A história começa na ponta escondida dos dentes em crescimento.
O que revelou o novo estudo
Investigadores da Universidade de Ciência de Tóquio e do Centro de Ciências da Saúde da Universidade do Texas mapearam a coreografia celular que constrói a raiz de um dente. Na Nature Communications a 1 de julho de 2025, relatam duas linhagens de células estaminais anteriormente ignoradas, que orientam a formação da raiz e ajudam a reparar o osso da mandíbula que segura os dentes no lugar.
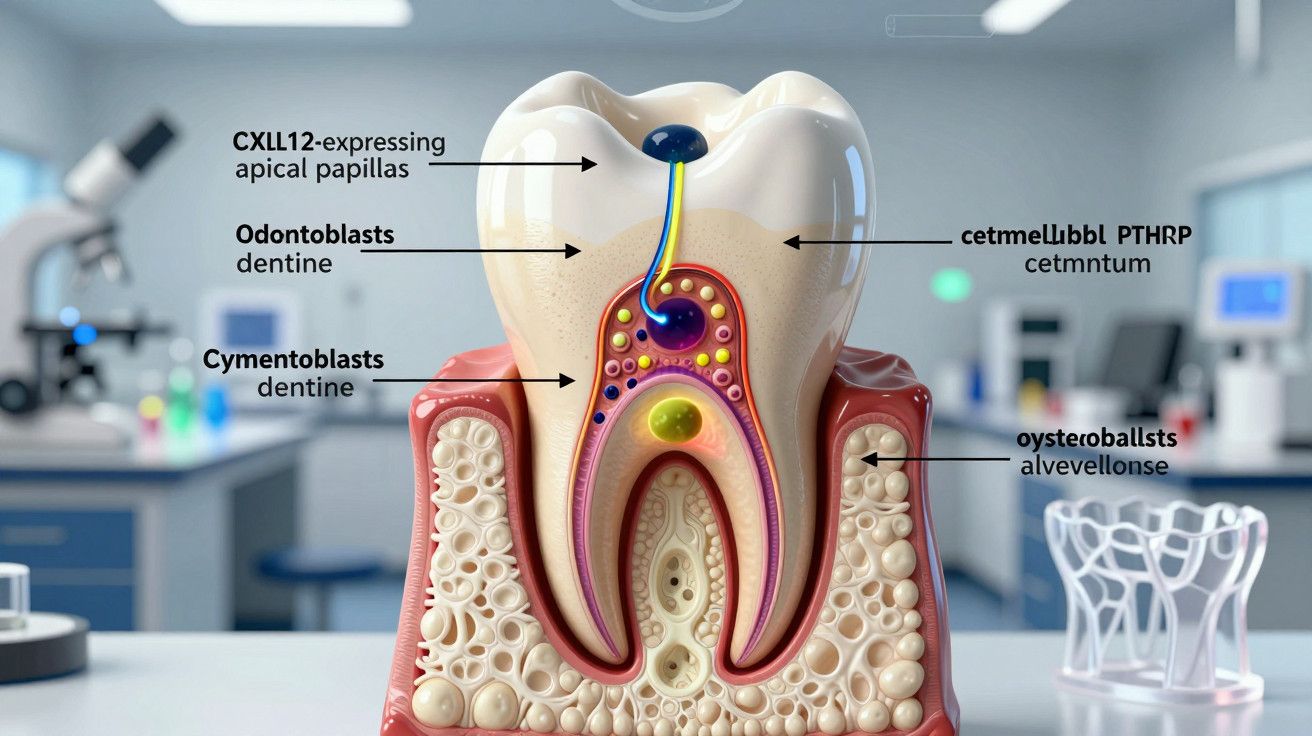
Duas populações distintas de células estaminais situam-se na ponta da raiz e à volta do dente em desenvolvimento, moldando a dentina, a cobertura radicular e o osso que ancora os dentes.
Duas linhagens de células estaminais, dois papéis
A primeira linhagem reside na papila apical, um bolso de tecido mole no final de uma raiz em crescimento. Estas células expressam CXCL12, uma proteína sinalizadora conhecida por guiar a migração celular e suportar a reparação óssea. A partir deste nicho, as células podem diferenciar-se em odontoblastos que produzem dentina, cementoblastos que revestem a raiz com cimento protetor, ou osteoblastos que constroem o osso alveolar quando é necessário reparação.
A segunda linhagem concentra-se no folículo dentário, um saco fibroso que envolve o germe dentário. Estas células expressam PTHrP, uma proteína relacionada com a hormona paratiroidea e há muito ligada ao crescimento ósseo e remodelação tecidular. No estudo, as células do folículo contribuíram sobretudo para o osso alveolar. Sob condições específicas que imitam a reparação, também se transformaram em cementoblastos, sugerindo uma reserva que as clínicas poderão recrutar durante a regeneração.
Como a equipa acompanhou as células
O grupo utilizou ratos geneticamente modificados, rastreamento fluorescente de linhagens e interruptores genéticos para seguir o movimento e o destino das células. A microscopia de alta resolução captou o crescimento das raízes ao longo do tempo. Ao ligar ou desligar sinais, os investigadores observaram como as pistas proteicas determinavam o destino das células durante a elongação da raiz e formação do alvéolo. Essa abordagem criou um mapa mecanístico de quais progenitores gerem a dentina, o cemento e o osso de suporte.
Porque isto importa para os doentes
Os implantes e pontes atuais restauram a mastigação e a aparência. Não recriam uma raiz e ligamento vivos. Muitos pacientes sentem uma mordida alterada e menor perceção sensorial. O osso da mandíbula pode tornar-se mais fino lentamente sem a tração microscópica de um ligamento natural.
- Uma raiz viva pode restabelecer vasos sanguíneos e nervos no interior da polpa.
- Cemento e ligamento periodontal restauram a absorção de choques e o controlo preciso da mordida.
- Osso alveolar regenerado suporta a estabilidade a longo prazo e reduz a perda óssea.
- A integração biológica pode reduzir o risco de inflamação crónica em torno dos dispositivos.
- Raízes em desenvolvimento poderão servir melhor os pacientes jovens cujas mandíbulas ainda estão a mudar de forma.
Regenerar uma bio-raiz visa restituir sensação, resiliência e manutenção do osso mandibular que os implantes protéticos não conseguem igualar totalmente.
Como poderá ser um tratamento futuro
O trabalho em ratos não fornece às clínicas uma terapia pronta a aplicar. Mas descreve os ingredientes que um dentista de próxima geração poderá combinar em ambiente controlado.
- Fonte: colher ou recrutar progenitores semelhantes à papila apical e ao folículo a partir do próprio paciente ou de um banco compatível.
- Sinais: administrar CXCL12 e PTHrP em impulsos temporizados para orientar as células para odontoblastos, cementoblastos ou osteoblastos conforme necessário.
- Suporte: matrizes 3D impressas e biorreabsorvíveis com a forma do canal radicular e alvéolo, com microcanais para vasos e nervos.
- Preparação em biorreator: pré-culturar a construção para iniciar as camadas de dentina e cemento antes da colocação.
- Colocação cirúrgica: inserir a raiz viva no alvéolo, reconectar a irrigação sanguínea e estabilizar com uma coroa temporária.
- Fase de remodelação: carregamento gradual do dente para permitir formação do ligamento e espessamento do osso onde há maior exigência.
Limitações e questões em aberto
- Diferença entre espécies: o crescimento radicular em ratos difere da anatomia e cronologia dos molares humanos.
- Controlo: os clínicos têm de evitar que as células migrem para fibrose ou excesso de formação óssea indesejada.
- Segurança: qualquer terapia com células estaminais exige controlos rigorosos para risco de tumores e reações imunológicas.
- Precisão: moldar uma raiz que se adapte a um canal e mordida únicos requer imagiologia e impressão avançadas.
- Durabilidade: polpa, dentina e ligamento regenerados têm de resistir anos de forças mastigatórias e pressão bacteriana.
- Acesso: custos, tempo em cadeira e comparticipação determinarão quem beneficia primeiro.
Como se compara com as opções atuais
| Opção | O que substitui | Pontos fortes | Limitações |
| Implante dentário | Raiz e coroa ausentes | Elevada taxa de sucesso, mastigação forte, cirurgia previsível | Sem ligamento ou sensação; risco de peri-implantite; a perda óssea pode continuar |
| Ponte | Coroa e vão ausentes | Restauração rápida, sem enxerto | Exige cortar dentes adjacentes; higiene difícil; sem função radicular |
| Desvitalização + coroa | Polpa infetada | Preserva o dente natural; bom conforto | Sem polpa viva; a raiz pode enfraquecer com o tempo |
| Bio-raiz regenerativa (experimental) | Raiz, ligamento e osso de suporte | Potencial para sensação, absorção de choques e preservação óssea | Ainda não disponível em clínicas; obstáculos de fabrico e segurança |
Sinais nos bastidores
O CXCL12 atua frequentemente como um sinal chamativo. Na reparação óssea, atrai progenitores a locais de lesão e ajuda no crescimento de vasos. A sua presença na papila apical encaixa num papel de recrutamento e orientação de novos odontoblastos ou osteoblastos à medida que a raiz se alonga.
O PTHrP influencia a divisão e maturação das células esqueléticas. No folículo dentário, o seu perfil sugere um interruptor que pode orientar as células estaminais para cementoblastos quando a superfície da raiz precisa de nova cobertura. Esse interruptor pode ser sensível à carga mecânica e à inflamação local, dois fatores importantes na periodontite e após extração dentária.
O que observar a seguir
As equipas tentarão repetir o rastreamento das linhagens em animais maiores com anatomia dentária mais próxima da humana. São esperados ensaios que combinem ambas as linhagens num único constructo para testar a coordenação entre dentina, cemento e osso. Estudos de imagiologia poderão seguir a orientação das fibras do ligamento durante a regeneração em resposta à mastigação.
Os clínicos também procuram biomarcadores para prever a cicatrização. Testes sanguíneos ou de saliva para atividade de CXCL12 ou PTHrP podem indicar quem responde melhor a um enxerto de bio-raiz. Para crianças com raízes pouco desenvolvidas, a regeneração guiada poderá salvar dentes da frente traumatizados sem necessidade de implantes de longa duração.
Contexto útil se estes termos são novos para si
- Papila apical: tecido mole na ponta da raiz que alimenta o alongamento radicular durante o desenvolvimento dentário tardio.
- Odontoblasto: célula que deposita dentina, o tecido duro sob o esmalte e ao longo da parede do canal radicular.
- Cementoblasto: célula responsável pela produção de cemento, a fina camada mineral que ancora as fibras do ligamento à raiz.
- Osteoblasto: célula formadora de osso; neste contexto, engrossa e repara o alvéolo dentário.
- Osso alveolar: o osso especializado da mandíbula que aloja os alvéolos dentários e se remodela com as forças da mastigação.
Se valoriza um impacto a curto prazo, esteja atento às terapias periodontais. Guiar a reparação de cemento e ligamento em torno de dentes abalados poderá chegar às clínicas antes de se conseguir gerar um dente bioartificial completo. Os mesmos sinais mapeados em ratos podem refinar enxertos ósseos, encurtar o tempo de cicatrização e estabilizar dentes em risco após limpezas profundas ou cirurgias.
A gestão de risco estará no centro de qualquer ensaio. Simulações já ajudam a planear a rigidez das matrizes e padrões de carga, reduzindo micromovimentos que podem prejudicar as fibras do ligamento. Os primeiros protocolos poderão combinar antibióticos de baixo dose, esquemas anti-inflamatórios e aplicação de carga gradual para proteger a janela de remodelação enquanto a nova raiz se integra.





Comentários (0)
Ainda não há comentários. Seja o primeiro!
Deixar um comentário